《医疗器械注册与备案管理办法》中第十条规定:国家药品监督管理局对临床急需医疗器械实行优先审批,对创新医疗器械实行特别审批,鼓励医疗器械的研究与创新,推动医疗器械产业高质量发展。
创新医疗器械由于产品具有显著的临床应用价值,在科技立项、融资、信贷、招标采购、医疗保险等方面具有较大意义。企业在申请医疗器械注册时,各级药监局予以创新医疗器械特别审批支持。那么,申请创新医疗器械对产品的注册周期和注册流程有哪些影响?
创新医疗器械的申请
具体如下:
什么是创新医疗器械?
创新医疗器械是国内没有同类产品注册,且具有显著的临床应用价值的新产品,创新医疗器械需要有以下几个特点:
- 产品确定是医疗器械,具有显著的临床应用价值,工作原理或作用机理明确。
- 申请人已完成申报产品的前期研究并具有基本定型产品,研究过程真实和受控,研究数据完整和可溯源。
- 具有技术创新和领先优势。
什么是技术创新和领先优势?
- 5年内在国内取得中国产品核心技术发明专利,或依法通过受让取得在中国发明专利权或其使用权。注意外观专利和实用型新专利不属于创新申请范围。
- 发明专利还在申请过程中,但申请已由国务院专利行政部门公开,并由国家知识产权局专利检索咨询中心出具检索报告,报告载明产品核心技术方案具备新颖性和创造性。
- 产品主要工作原理或作用机理为国内首创,产品性能或者安全性与同类产品比较有根本性改进,技术为国内领先。
创新医疗器械申报流程
申请人将创新医疗器械申报资料提交给所在地省级药品监督管理部门,由该部门对资料进行审核,二类产品符合要求的准予通过创新审查,三类产品提交给国家药监局进行审理,流程如下:
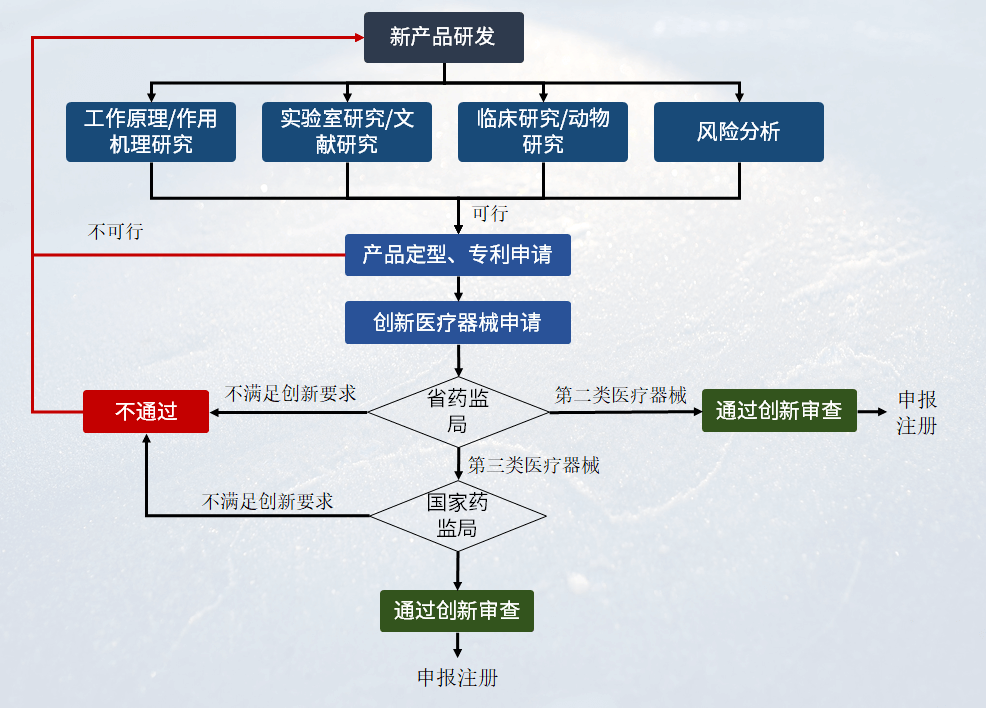
图1 创新医疗器械申报流程
各省市创新医疗器械申请材料略有差异,依据《创新医疗器械特别审查申报资料编写指南》(2018年第127号),国内医疗器械生产企业申请材料见下表:
表1 创新医疗器械特别审查申请材料
| 序号 | 资料要求 | 说明 |
| 1 | 创新医疗器械特别审查申请表 | / |
| 2 | 申请人企业资质证明文件 | 企业营业执照复印件 |
| 3 | 医疗器械的分类依据 | 分类目录说明、分类界定结果 |
| 4 | 产品知识产权情况及证明文件 | 发明专利证书、查新报告等 |
| 6 | 产品研发过程及结果的综述 | 综述产品研发的立题依据及已开展的各项研究 |
| 6 | 产品技术文件 | 产品的预期用途/适用范围 |
| 产品工作原理/作用机理说明 | ||
| 产品主要技术指标及确定依据 | ||
| 主要原材料、关键元器件的指标要求 | ||
| 主要生产工艺过程及流程图 | ||
| 主要技术指标的检验方法 | ||
| 7 | 产品说明书 | 说明书样稿 |
| 8 | 体现临床应用价值的资料 | 阐述产品的创新内容,论述通过创新使所申请医疗器械较现有产品或治疗手段在安全、有效、节约等方面发生根本性改进和具有显著临床应用价值。以及支持性资料。 |
| 9 | 风险分析资料 | 风险分析报告 |
| 10 | 其他证明性资料 | 产品获得省级、国家级科技创新奖励 |
| 11 | 资料真实性自我保证声明 | / |
创新医疗器械申请情况
具体如下:
第三类医疗器械
第三类创新医疗器械即为“国家创新”,自2014年第一个创新医疗器械注册以来,截止2023年8月10日,总局已批准224个第三类创新医疗器械产品,涵盖重离子治疗系统、质子治疗系统、手术机器人、人工血管等诸多高端医疗器械。已注册产品目录可由国家药监局官网查询。
从各省的已注册的第三类创新医疗器械数量来看,京、沪、粤、苏、浙五省占80%以上的申请数量,这也和国内医疗器械生产企业的分布一致。
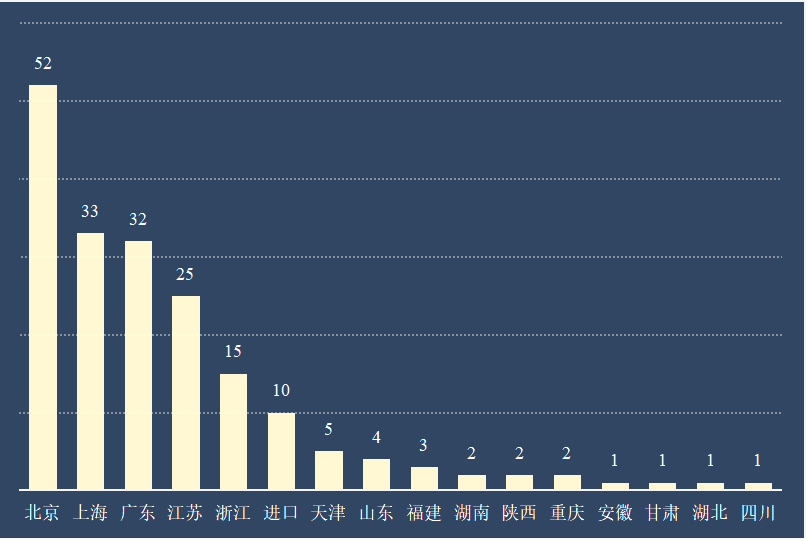
图2 各省已注册的创新医疗器械数量(2014-2022)
从每年已注册的产品数量来看,创新医疗器械的数量一直程稳步增长的状态,其中部分原因是进入特别审查程序的医疗器械注册有1-3年的时间差。
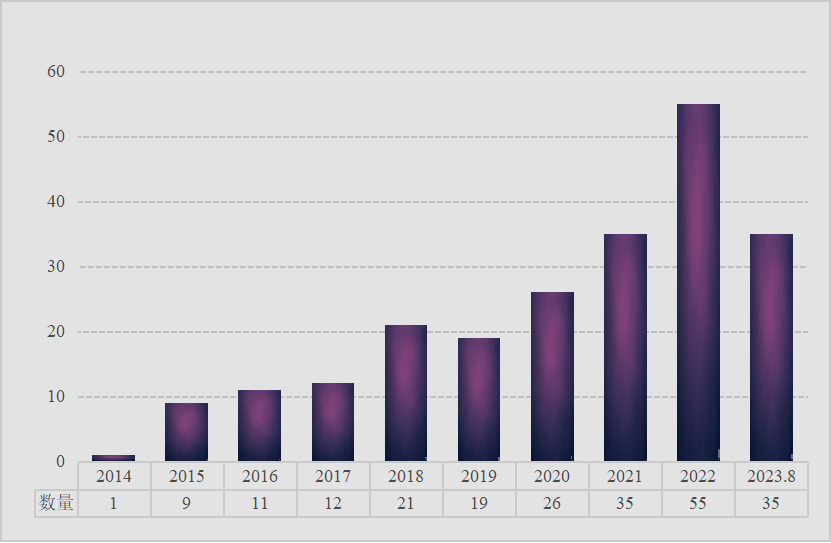
图3 年度已注册的创新医疗器械数量
第二类医疗器械
第二类创新医疗器械即为“省创新”,由各省、自治区和直辖市药监局进行创新申请和注册。以浙江省为例,自2016以来,共有83个产品进入创新医疗器械特别审查程序,其中有40个产品已取得注册证,其余产品可能正在注册申请的过程中或厂家已放弃注册。产品目录见下表:
表2 浙江省创新医疗器械目录
| 序号 | 产品名称 | 创新批准日期 | 注册情况 | 注册证号 |
| 1 | 脑部电阻抗断层成像仪 | 2016.11.09 | 杭州永川科技有限公司 | 浙械注准20172070633 |
| 2 | 自动乳腺超声系统 | 2016.11.14 | 嘉兴深博医疗器械有限公司 | / |
| 3 | 弱视治疗仪 | 2016.12.08 | 杭州瑞杰珑科技有限公司 | / |
| 4 | 激光定位系统 | 2017.01.10 | 杭州三坛医疗科技有限公司 | 浙械注准20172040913 |
| 5 | 外骨骼助行器 | 2017.01.10 | 宁波顶峰机器人有限公司 | / |
| 6 | 电鍉针治疗仪 | 2017.04.07 | 浙江思科博瑞医疗科技有限公司 | / |
| 7 | 肝素结合蛋白测定试剂盒(免疫荧光干式定量法) | 2017.04.17 | 中翰盛泰生物技术股份有限公司 | / |
| 8 | 病理切片组织成像系统 | 2017.05.31 | 杭州筹图科技有限公司 | / |
| 9 | 体液平衡监测仪 | 2017.06.05 | 浙江新蓝科技有限公司 | / |
| 10 | 膀胱刺激电极 | 2017.06.14 | 杭州承诺医疗科技有限公司 | 浙械注准20222090046 |
| 11 | 牙科种植用钻头(横孔出水内冷却) | 2017.07.31 | 绍兴华晶科技有限公司 | / |
| 12 | 肺功能测定仪 | 2017.08.16 | 台州亿联健医疗科技有限公司 | / |
| 13 | 射频治疗仪 | 2017.09.13 | 杭州瑞彼加医疗科技有限公司 | 浙械注准20202090909 |
| 14 | 无创连续每搏动脉血压监测系统 | 2017.11.03 | 浙江脉联医疗设备有限公司 | 浙械注准20192070148 |
| 15 | 沸石粉状敷料 | 2017.12.01 | 杭州沸创医疗科技有限公司 | / |
| 16 | 液囊肠梗阻导管 | 2017.12.13 | 浙江迅康医疗器械有限公司 | / |
| 17 | 肺部CT辅助分析/检测软件 | 2018.05.25 | 杭州健培科技有限公司 | 浙械注准20212210193 |
| 18 | 一次性使用无菌三用喷枪枪头 | 2018.06.12 | 杭州瑞岚得医疗科技有限公司 | 浙械注准20192170428 |
| 19 | 血压计 | 2018.06.28 | 杭州柯氏音医疗器械有限公司 | 浙械注准20202070510 |
| 20 | 牙科手机用一次性使用无菌口腔冲洗器 | 2018.08.13 | 杭州瑞岚得医疗科技有限公司 | 浙械注准20192170429 |
| 21 | 全自动核酸检测反应体系构建系统 | 2018.09.14 | 杭州杰毅麦特医疗器械有限公司 | 浙械注准20202220328 |
| 22 | 可视气管插管 | 2018.09.30 | 浙江百益医疗科技有限公司 | 浙械注准20202080719 |
| 23 | 封闭式人卵母细胞或胚胎玻璃化冷冻贮存装置 | 2018.10.18 | 浙江安久生物科技有限公司 | 浙械注准20232180028 |
| 24 | 平衡机能检测分析仪 | 2018.11.27 | 杭州拜伦医疗科技有限公司 | 浙械注准20202070730 |
| 25 | 全自动过敏原IgE抗体分析仪 | 2018.12.10 | 浙江蓝怡医药有限公司 | 浙械注准20192220443 |
| 26 | 经皮暨穴位治疗仪 | 2019.01.25 | 杭州大力神医疗器械有限公司 | 浙械注准20222201168 |
| 27 | 硬膜压贴三棱镜斜视矫正眼镜 | 2019.04.01 | 浙江安百乐生物科技有限公司 | / |
| 28 | CT无创血流储备分数测量系统 | 2019.05.14 | 杭州阿特瑞科技有限公司 | / |
| 29 | 流式点阵发光分析仪 | 2019.06.17 | 中翰盛泰生物技术股份有限公司 | 浙械注准20212220285 |
| 30 | 显微授精操作皿 | 2019.07.12 | 杭州德适生物科技有限公司 | 浙械注准20202180455 |
| 31 | 磁感应脑电阻抗成像仪 | 2019.08.15 | 杭州永川科技有限公司 | / |
| 32 | 消化道黏膜创面保护胶 | 2019.09.23 | 杭州英健生物科技有限公司 | 浙械注准20222140160 |
| 33 | 干眼综合治疗仪 | 2019.09.23 | 浙江花园润嘉医疗器械有限公司 | 浙械注准20212160213 |
| 34 | 胎儿/母体心率记录仪 | 2019.11.18 | 浙江荷清柔性电子技术有限公司 | 浙械注准20212070121 |
| 35 | 内镜吻合夹 | 2019.11.25 | 宁波胜杰康生物科技有限公司 | 浙械注准20222020390 |
| 36 | 一次性使用表皮细胞分离器 | 2019.12.12 | 振德医疗用品股份有限公司 | 浙械注准20202220658 |
| 37 | 下肢外骨骼步行康复器 | 2020.01.10 | 杭州程天科技发展有限公司 | 浙械注准20202190269 |
| 38 | 一次性使用前房穿刺器 | 2020.01.21 | 杭州华视诺维医疗科技有限公司 | 浙械注准20222160372 |
| 39 | 中枢神经系统脱髓鞘三项(AQP4, MOG, MBP)自身抗体检测试剂盒(细胞免疫荧光法) | 2020.03.03 | 浙江达美生物技术有限公司 | / |
| 40 | 中枢神经系统脱髓鞘(AQP4)自身抗体检测试剂盒(细胞免疫荧光法) | 2020.03.03 | 浙江达美生物技术有限公司 | / |
| 41 | 食物特异性抗体IgG4检测试剂盒(蛋白芯片法) | 2020.03.11 | 杭州浙大迪迅生物基因工程有限公司 | 浙械注准20202400759 |
| 42 | 双通道扩张导引鞘套件 | 2020.04.20 | 海盐康源医疗器械有限公司 | / |
| 43 | 骨折复位辅助系统 | 2020.06.17 | 浙江九微医疗科技有限公司 | / |
| 44 | 沸石止血纱布 | 2020.06.30 | 杭州沸创医疗科技有限公司 | / |
| 45 | 细菌药敏试剂盒系列:革兰氏阴性菌检测试剂盒(微量肉汤稀释法) | 2020.07.29 | 杭州伽玛生物科技有限公司 | / |
| 46 | 心率变异分析仪 | 2020.07.31 | 杭州菲诗奥医疗科技有限公司 | 浙械注准20212070074 |
| 47 | 精子梯度离心管 | 2020.09.15 | 艾尔斯(浙江)医学科技有限公司 | 浙械注准20222180400 |
| 48 | 捡卵管 | 2020.09.15 | 艾尔斯(浙江)医学科技有限公司 | 浙械注准20222180401 |
| 49 | 一次性使用肺外科标记物 | 2020.09.24 | 杭州堃博生物科技有限公司 | 浙械注准20212020245 |
| 50 | 自动调节低频治疗仪 | 2020.12.07 | 丽水澳中医疗设备有限公司 | / |
| 51 | 食管肠道黏膜创面保护胶 | 2021.01.11 | 杭州英健生物科技有限公司 | 浙械注准20222140194 |
| 52 | 胸腔引流监控系统 | 2021.03.08 | 浙江乐信医疗科技有限公司 | 浙械注准20222140139 |
| 53 | 胸腹腔镜 | 2021.03.15 | 杭州首天光电技术有限公司 | / |
| 54 | 非吸收高分子结扎夹用连发施夹钳 | 2021.04.25 | 杭州圣石科技股份有限公司 | 浙械注准20232021017 |
| 55 | 液相色谱串联质谱系统 | 2021.06.16 | 杭州谱聚医疗科技有限公司 | 浙械注准20222220115 |
| 56 | 脑卒中风险辅助筛查软件 | 2021.06.28 | 浙江达美生物技术有限公司 | 浙械注准20222221072 |
| 57 | 尘螨组分特异性抗体IgE检测试剂盒(蛋白芯片法) | 2021.07.30 | 杭州浙大迪迅生物基因工程有限公司 | / |
| 58 | 尘螨组分特异性抗体IgG4检测试剂盒(蛋白芯片法) | 2021.07.30 | 杭州浙大迪迅生物基因工程有限公司 | / |
| 59 | 数字胸腔引流系统 | 2021.08.16 | 宁波新跃医疗科技股份有限公司 | / |
| 60 | 一次性使用ERCP电子内窥镜 | 2021.08.20 | 杭州莱恩瑟特医疗技术有限公司 | / |
| 61 | 颅内医学图像处理软件 | 2021.09.10 | 杭州脉流科技有限公司 | 浙械注准20212210431 |
| 62 | 心磁图仪 | 2021.11.24 | 杭州诺驰生命科学有限公司 | 浙械注准20222071226 |
| 63 | 3D电子胸腹腔镜 | 2021.11.29 | 赛诺微医疗科技(浙江)有限公司 | 浙械注准20222060187 |
| 64 | 仿生假手 | 2021.12.06 | 浙江强脑科技有限公司 | / |
| 65 | 一次性使用腔内闭式镜头清洗穿刺器 | 2022.01.27 | 宁波海泰科迈医疗器械有限公司 | / |
| 66 | 可视单腔支气管插管 | 2022.02.08 | 昊谱(杭州)生物科技有限公司 | / |
| 67 | 穿戴式经皮胫神经刺激器 | 2022.03.14 | 杭州承诺医疗科技有限公司 | / |
| 68 | 微纳孔骨牵引针 | 2022.03.15 | 浙江科惠医疗器械股份有限公司 | 浙械注准20222041192 |
| 69 | 沉浸式儿童注意力缺陷与多动障碍康复训练软件 | 2022.06.06 | 浙江凡聚科技有限公司 | / |
| 70 | 抗磷脂酶A2受体抗体IgG4检测试剂盒(时间分辨荧光免疫分析法) | 2022.06.06 | 浙江博实生物科技有限公司 | 浙械注准20222400361 |
| 71 | 高倍率放大电子上消化道内窥镜 | 2022.06.17 | 浙江之科立上医疗科技有限公司 | / |
| 72 | 外科机械臂腔镜手术器械 | 2022.09.05 | 杭州康基医疗器械有限公司 | 浙械注准20222021285 |
| 73 | 肺功能呼气分析一体机 | 2022.09.23 | 浙江亿联康医疗科技有限公司 | / |
| 74 | 手术显微镜3D数字化成像观察系统 | 2022.10.28 | 嘉兴智瞳科技有限公司 | / |
| 75 | 一次性激光眼保护敷料 | 2022.11.03 | 杭州炬九生物科技有限公司 | / |
| 76 | 一次性使用可旋转多通道腹腔镜手术单孔穿刺器 | 2023.01.13 | 杭州康基医疗器械有限公司 | / |
| 77 | 血管内皮生长因子A(VEGF-A)测定试剂盒(磁微粒化学发光法) | 2023.02.09 | 杭州华视诺维医疗科技有限公司 | / |
| 78 | 一次性使用球囊套管穿刺器 | 2023.02.13 | 杭州康基医疗器械有限公司 | / |
| 79 | 医用智能介入射线防护减负系统 | 2023.02.17 | 融仁(杭州)医疗器械有限公司 | / |
| 80 | 主客一体双眼波前验光仪 | 2023.03.17 | 浙江爱至瞳医疗科技有限公司 | / |
| 81 | 激光消融光纤套件 | 2023.03.24 | 杭州佳量医疗科技有限公司 | / |
| 82 | 一次性使用夹子装置 | 2023.04.04 | 宁波新跃医疗科技股份有限公司 | / |
| 83 | 一次性使用半板缝合枪 | 2023.06.25 | 杭州锐健马斯汀医疗器材有限公司 | / |
产品进入创新审查程序是否利于注册
常规来说,进入创新医疗器械审查程序的产品不代表已认定产品具备可获准注册的安全有效性,申请人仍需按照有关要求开展研发及提出注册申请,各级药品监督管理部门及相关技术机构将按照早期介入、专人负责、科学审查的原则,在标准不降低、程序不减少的前提下进行审评审批。
因此,创新医疗器械在注册时,并不能减少注册审批的流程,反之,由于创新医疗器械无法找到已注册的同类产品,临床评价难以通过豁免途径或同品种比对的路径进行评价。优缺点对比可见下表:
表3 创新医疗器械优缺点对比表
| 项目 | 创新医疗器械 | 常规医疗器械 |
| 临床价值 | 高 | 普通 |
| 产品风险 | 可能存在未知风险 | 风险相对较明确 |
| 产品检测 | 需要检测 | 需要检测 |
| 临床评价 | 难以豁免临床试验 | 部分产品可豁免或通过同类产品对比 |
| 注册周期 | 较长 | 适中 |
| 注册难度 | 较难 | 适中 |
| 医保目录 | 一般不在目录中 | 较大概率在目录中 |
| 融资信贷 | 较容易 | 一般 |
| 招标采购 | 竞争少 | 一般 |
| 政策扶持 | 多 | 一般 |
